
Autor: Eulalia Maria Amador Rodero
Titulo: Neurotransmisores Moleculares
Area:
Pais: Colombia
Perfil:
Programa:
Disponible para descarga: Yes
Ver Más Publicaciones Estudiantiles Clic aquí
Diseminar información, ideas innovadoras y conocimientos académicos es una función importante para Atlantic Internacional University. Publicaremos noticias, artículos, comentarios y otras publicaciones de nuestros estudiantes y otros colaboradores. Si desea contactar al autor por motivos profesionales favor enviar su petición por este medio.
Para conocer más de la iniciativa de Acceso Abierto de AIU haga Clic aquí.
INTRODUCCIÓN
Los
neurotransmisores son sustancias químicas que se encargan de la transmisión de
las señales desde una neurona hasta la siguiente a través del mecanismo llamado
sinápsis. Estas sustancias también se encuentran en la terminal axónica de las
neuronas motoras, en el lugar donde inervan al músculo. Son elaborados en el
cuerpo de la neurona, en algunas glándulas como la hipófisis, y adrenal.
Estas
vias serotoninérgicas se expanden ampliamente a través del tronco encefálico,
corteza cerebral y médula espinal. Además de controlar el estado anímico, se ha
asociado con una amplia variedad de funciones, incluida la regulación del
sueño, la percepción del dolor, la temperatura corporal, la tensión arterial y
la actividad hormonal. Fuera del cerebro tiene efecto sobre los sistemas
gastrointestinal y cardiovascular.
La
histamina se encuentra distribuída ampliamente en el reino animal pero de
manera desigual. Se encuentra de manera abundante en la mucosa del árbol
bronquial y del tracto digestivo. Interviene en las respuestas de
hipersensibilidad inmediata y alérgica. Recientemente se ha identificado su
función como neurotransmisor del sistema nervioso central.
1. SINAPSIS.
Algunos
neurotransmisores como la acetil colina (ACh), la glicina, glutamato,
aspartato, y ácido gamma-amino-butírico (GABA), aumentan la conductancia a
ciertos iones por adherencia a canales iónicos en la membrana postsináptica.
Otros neurotransmisores como la noradrenalina (NA), dopamina (DA) y serotonina (5.HT) no tienen una actividad directa, sino
indirecta a través de un segundo mensajero para generar una respuesta
post-sináptica. Estos segundos mensajeros son el Adenosin-monofosfato-cíclico
(AMPc), Guanidín-monofosfato-cíclico (CMPc), Inositol-trifosfato (ITP),
Diacil-glicero (DAG), Prostaglandinas (Pgs), Leucotriénos, epóxidos y calcio
Ca++.
Una
característica diferencial de los neurotransmisores es que su efecto depende
del receptor postsinaptico que lo recibe, y estos al ser distintos dentro de la
misma neurona hacen que no sea fácil la predicción de las consecuencias.
La
Ach fue el primer nerutransmisor identificado en el sistema nervioso central.
Para ello fue fundamental el principio de
Sir Henry Dale, cuando una
neurona colinérgica ó adrenérgica experimenta regeneración el transmisor
original es reestablecido y es inalterable. Parte del principio de Dale se
aplica a las neuronas periféricas y centrales. El principio de Dale aunque
básico, no se mantiene por que cada vez son mas las sustancias que coexisten
con el neurotransmisor clásico como aminas primarias, histamina, octamina,
feniletilemina, feniletanolamina, y poliaminas como espermina y espermidina,
también aminoácidos, ácido glutámico y ácido aspártico, glicina y Betaalanina, GABA,
taurina y prolina. Otras moléculas pequeñas son sugeridas como
neurotransmisores; estas moléculas son Ca++. ATP, AMPc, GTP, GTPc, Citidín
trifosfato, estrógenos, progesterona, testosterona, corticosterona, y varias
prostaglandina.
El
neurotransmisor es una sustancia química, que interviene en la transmisión de
los impulsos nerviosos, en las uniones sinápticas, entre una neurona y otra ó
entre una neurona y la estructura que inerva.
Los
neurotransmisores son elaborados en el cuerpo de las neuronas, de allí son
conducidos hasta las terminales presinápticas, en estas son almacenados en
forma de vesículas.
Los
receptores son los componentes de una célula capaz de identificar una
sustancia, hormona ó neurotransmisor. La
actividad de los neurotransmisores está relacionada con la interacción de un
número relacionado de familias de receptores: los ligados a la apertura de
canales iónicos, los relacionados con la proteína G, factor de crecimiento que
tienen actividad tirosina kinasa y los receptores esteroides que son
macromoléculas intracelulares que funcionan para transportar esteroides dentro
del núcleo donde actúan para modular la actividad transcriptora.
Los
ligados a apertura de canales iónicos de apertura son receptores heteroméricos
que contienen muchas unidades. El prototipo de estos receptores es el
colnérgico nicotínico el cual tiene 5 subunidades alfa, beta, delta y gamma. De
los asociados a la Proteina G se encuentra el receptor betaadrenérgico. Los
receptores de esta familia tienen secuencias y semejanzas en su estructura como
con los pigmentos de rodopsina y opsina, se cree que estas proteínas tienen
siete hélices con un terminal amino extracelular para la glocosilación y un
terminal carboxiintracelular para la fosforilación.
La
forma mas sencilla de entender lo que sucede en un botón terminal es observar
una sinápsis in Vitro. Este consiste en una estructura cerrada de una membrana
plasmática intacta la cual mantiene una bomba activa de sodio con el aporte de
glucosa, igual que en un botón terminal, es decir que la salida del Na+
conlleva a la acumulación de K+. El fenómeno mas representativo es la
liberación del neurotransmisor, dependiente del calcio
Por
esta razón las investigaciones últimamente tienden a basarse en los mecanismos
de acción de los antagonistas del calcio ya que son de los más importantes en
la terapéutica y prevención de enfermedades cerebrovasculares y trastornos
circulatorios.
1.2.1. REGULACIÓN DE LA SINTESIS DEL
NEUROTRANSMISOR.
Un
botón terminal mantiene una polarización de la membrana celular y una
regulación de la capacidad de síntesis del neurotransmisor deacuerdo con las
exigencias funcionales de la neurona y de su control metabólico. Esto quiere
decir que la conducción de un impulso nervioso rompe el esfuerzo fisiológico
para mantener la polarización de la membrana, produce una significativa
movilización de vesículas sinápticas que almacenan neurotransmisores, los
cuales se unen a la propia membrana plasmática, la entrada de Ca++ como
consecuencia de la despolarización, que abre los canales de calcio, rompe la
anastomosis vesícula membrana y libera al espacio sináptico al neurotransmisor.
1.2.2. LIBERACION DEL NEUROTRANSMISOR.
Cuando
el neurotransmisor es liberado en el espacio sináptico, este sigue las
siguientes rutas:
· Fijación
en los espacios presinápticos y postsinapticos, es decir en los receptores de
la membrana celular.
· Se
dispersa en el espacio sináptico y actúa como un modulador.
· El neurotransmisor es recaptado.
· Catabolización
del neurotransmisor y por lo tanto este se degrada.
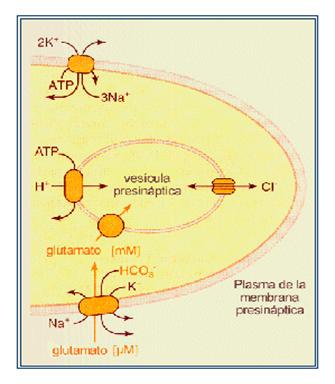
Figura 1: Recaptación
de neurotransmisores. Tomado de Siegel, G. J (ed.): "Basic Neurochemistry
1.2.3. ACTIVACION DE RECEPTORES POSTSINAPTICOS.
Las
estructuras de unión del neurotransmisor con la membrana postsináptica son
proteínas específicas de membrana que constituyen los receptores postsinapticos
y que son la clave del reconocimiento de la liberación de neurotransmisores
presinápticos. Esto quiere decir que los receptores postsinapticos son la
estructura básica para interpretar la
comunicación interneural, constituyen auténticas estructuras de diferenciación
neuronal a la vez que son un exponente de la diversidad específica.
La
afinidad del neurotransmisor por el receptor postsináptico es una
característica inherente a la especialización y diferenciación de la neurona
hasta el punto de que un neurotransmisor no produce efectos por muy constante y
é intensa que sea su liberación, si la membrana no contiene en su
diferenciación los receptores específicos para ese neurotransmisor concreto. Cuando
el receptor y el neurotransmisor se unen, aparece inmediatamente una
consecuencia en la membrana postsináptica. Hay una modificación en su
constitución que puede ser suficiente para modificar los canales iónicos de
polarización de esa membrana, generando inmediatamente una despolarización ó
una hiperpolarización, lo que conduciría a un aumento de la activación ó
inhibición, respectivamente, de la membrana postsináptica. Normalmente la
activación de una membrana postsináptica es interpretada por la utilización de
un neuromediador ó de un segundo mensajero. Cuando es interpretada por un
neuromediador la acción neurotransmisor - receptor requiere de una proteína de membrana
mediadora ante la modificación de su permeabilidad iónica, ó hacia la
alteración de su polarización. Cuando es interpretado por un segundo mensajero
ya sea por la neuromediación ó por el complejo neurotransmisor-receptor se
activa un sistema enzimático de membrana, generalmente la adenilato-ciclasa,
cuya actuación se realiza sobre el Adenosin trifosfato (ATP) que se transforma
en Adenosin Monofosfato Cíclico (ATPc).
Este además de activar la apertura los canales iónicos conduce la
actividad de la membrana de la cual procede hacia las estructuras somáticas y
nucleares de la neurona, lo que hace que
las consecuencias de la comunicación interneuronal puede trascender a
mecanismos bioquímicos, los cuales implican cambios estructurales y/o
funcionales partir de la utilización del
segundo mensajero.
1.2.3.1. ACTIVACION DE RECEPTORES PRESINAPTICOS O
AUTORECEPTORES.
Es
importante la activación de receptores de membrana presinápticos los cuales
responden de la misma manera que lo hacen los receptores postsinapticos. El
resultado de esta actividad es la autorregulación de la liberación del neurotransmisor
para que la comunicación neuronal sea eficaz, y esté adecuada a los niveles de
excitabilidad que han provocado los potenciales de acción en los botones
terminales. Estos receptores no controlan canales iónicos. Regulan la
movilización de las vesículas, intervienen esencialmente en la disponibilidad
del neurotransmisor por consiguiente en su síntesis y liberación.
1.2.4. INACTIVACIÓN DEL NEUROTRANSMISOR.
Inmediatamente
que se produce la comunicación postsináptica ocurre la inactivación del neurotransmisor.
El mecanismo de inactivación más importante es la recaptación presinàptica.
Esto ocurre gracias a los transportadores de membrana quienes se encargan de
ubicarlos nuevamente en el espacio presinàptico. Estos transportadores actúan
de dos formas: ya sea sobre el neurotransmisor liberado y reconocido por su
transportador ó actuando sobre un
metabolito
intermediario resultado del mecanismo de catabolización de sistemas enzimáticos
postsinapticos. La recaptación ó degradación metabólica del neurotransmisor
termina con la activación de los receptores de membrana y por consiguiente
termina con la actividad del neurotransmisor.
1.2.5. DIFUSIÓN DEL NEUROTRANSMISOR.
La
última etapa de la sinápsis es la difusión del neurotransmisor. La naturaleza
de la materia transmisora en realidad no es quien define el efecto
postsináptico de la neurotransmisión, por el contrario son los canales iónicos
controlados por los receptores de la membrana postsináptica quienes definen el
efecto exitatorio ó inhibitorio; por consiguiente podemos encontrarnos con
efectos inhibitorios a un neurotransmisor exitatorio.
Las
múltiples etapas descritas en la sinápsis y los distintos mecanismos que
intervienen confirman que la sinápsis es la estructura más lábil por
consiguiente modificable del sistema Nervioso.
La
primera etapa es la síntesis del neurotransmisor. La regulación de la síntesis
es una actividad dependiente del núcleo y por consiguiente de la constitución y
diferenciación neuronal. En ella intervienen varios factores: el primero es la
presencia de precursores; el segundo la
activación de los sistemas enzimáticos; el tercero la propia concentración de
neurotransmisores. Conociendo este mecanismo se puede determinar el efecto
sinápticos mediante la utilización de productos exógenos que puedan afectar
algunas de las condiciones que se dan en esta etapa.
La
segunda etapa que corresponde a la liberación, está relacionada con la
anterior. Pero también está relacionada con los mecanismos que la provocan, los
efectos sobre la propagación del potencial de acción en el botó terminal y
especialmente sobre la concentración de Ca++ extracelular son importantes por
lo que los agonistas y antagonistas de Ca++ son altamente efectivo.
La
tercera etapa la de recepción, es la de mayor repercusión, no solo por que
inciden sobre los autoreceptores y postreceptores sino por la compenetración
con el neurotransmisor concreto. Por ejemplo en la acetil colina se definen los
efectos como nicotínicos y muscarínicos que tienen que ver con el efecto
colinérgico de la nicotina y la muscarina sobre distintos receptores
postsinapticos.
En
la cuarta etapa relacionada con la recaptación y degradación enzimática de los
neurotransmisores un ejemplo es el efecto de la cocaína, la cual tiene afinidad
por las proteínas transportadoras de adrenalina y bloquea la recaptación de
monoamina, esto hace que se intensifiquen los efectos por mantenerse mas tiempo
en el espacio sináptico.
2. CLASIFICACION
DE LOS NEUROTRANSMISORES.
El
sistema nervioso utiliza una gran variedad
de neurotransmisores, los cuales se pueden agrupar en familias. Dentro
de éstas familias tenemos:
2.1.
AMINOACIDOS EXITATORIOS.
2.1.1.
GLUTAMATO
Son los principales neurotransmisores
exitatorios del sistema nervioso central, en la mayoría de las sinápsis
mantienen la actividad continua, el principal aminoácido exitatorio es el
glutamato.
Sus receptores ionotrópicos son el n-metil-D-
aspartato (NMDA) y no (NMDA) este último asociado al canal de calcio puede ser
importante en la generación de la Potenciación De larga Duración PDL.
La PDL es un aumento en la potencia de la
transmisión sináptica como consecuencia del uso repetitivo que dura más de unos
minutos; en el hipocampo puede ser provocada por una actividad
sináptica de más de un segundo y puede persistir por tiempos prolongados de más
de una hora. El potencial de larga duración puede activarse desde cualquier
sitio del sistema nervioso pero especialmente del hipocampo, por eso éste ha
sido considerado como una estructura importante en la adquisición de la
memoria.
El modelo de PDL actual es el
siguiente:
·
Una
actividad aferente produce la liberación de glutamato desde el Terminal
presinàptico. (etapa 1)
·
El
glutamato liberado se une entonces a los receptores NMDA Y no NMDA de la
membrana postsináptica. Estos receptores provocan la entrada de Na+ (etapa 2)
lo cual despolariza la membrana postsináptica(etapa3)
·
La
despolarización de la membrana postsináptica además de producir un potencial
postsinaptico exitatorio PPSE expulsa el Mg2+del receptor NMDA asociado al
canal iónico (etapa4). El Mg2+ normalmente bloquea el receptor NMDA asociado al
canal iónico por consiguiente se desplaza como respuesta a la despolarización
postsináptica permitiendo la entrada adicional de Na+ y de Ca2+ en la célula
postsináptica (etapa5).
·
La
entrada de Ca2+ activa la proteína cinasa postsináptica (etapa 6), la cual es
responsable de la inducción de la PLD inicial, que es un fenómeno
postsinaptico.
·
El
mantenimiento de la PLD, además de requerir la activación continua de la
proteina cinasa (etapa 7a), necesita también una modificación de la liberación
del neurotransmisor (etapa 7b), es decir un aumento en la liberación como
respuesta a un impulso aferente. Este aumento, si bien es necesario para el
mantenimiento de la PDL, significa que la célula postsináptica debe producir
una señal secundaria difusible que pueda actuar sobre el Terminal
presinàptico.
Existe otro grupo de receptores de
glutamato asociados a proteínas G, estos son los receptores metabotrópicos, estos
receptores están relacionados con la depresión de larga duración del hipocampo
DLD.
El ácido glutámico y el ácido
aspártico son mediadores en la mayoría de las transmisiones sinápticas
exitatorias del cerebro están
involucrados en procesos cerebrales como la epilepsia, las lesiones cerebrales
isquémicas y el aprendizaje influyendo en las conexiones sinápticas
normales. Las interrelaciones cortico-talámicas, cortico-estriadas y límbicas son
profusas, es probable que una hiperactividad de estas interrelaciones puedan
generar alteraciones como las que se encuentran en la enfermedad de alzheimer.
El glutamato y sus enlaces además de
sus efectos exitatorios en los receptores de glutamato, son neurotoxinas
potentes. Existe una estrecha correlación entre potencia neurotóxica y afinidad
de los receptores de glutamato por una variedad de agonistas. Entre mayor
capacidad tiene un compuesto de producir despolarización de una membrana, mayor
probabilidad tiene de producir toxicidad de la misma.
Períodos prolongados de daños anóxico
en tejido neuronal conducen a un daño celular isquémico y neurotoxicidad. La
deficiencia de oxigeno precipita una reducción en los almacenes de energía
dentro de los compartimientos neuronales y de las células gliales con acidosis
y liberación de radicales libres. La disminución de los almacenes de energía
afecta el metabolismo celular, a las bombas iónicas que dependen de la energía y
a la capacidad de la célula de mantener un potencial de membrana en reposo. La
despolarización de las células conduce a potenciales de acción y a la
liberación de glutamato en las terminales presinápticos. El glutamato liberado
activa al a-amino-3-hidroxi-5-metil-4- isoxazoleprolepropiónico (AMPA)
postsinaptico y a los receptores de NMDA. La entrada de Ca2+ a través del
complejo receptor de NMDA y los canales de Ca2+ sensibles al voltaje aumentan
la concentración de ca2+ intracelular. Estos desencadenan una cascada de
segundos mensajeros los cuales permanecen activado mucho tiempo después de que
el estímulo ha cesado. La incapacidad de un grupo de células de mantener un
potencial de reposo, acelera un bucle de retroalimentación positiva que lleva a
la muerte ó daño celular. La utilización por ejemplo de u n bloqueador del receptor del NMDA, produce una protección
del hipocampo y del estriado, dos de las regiones mas frecuentemente dañadas
por la interrupción del riego sanguíneo.
Los aminoácidos también tienen su
implicación en las formas de epilepsia. La actividad epileptiforme es
normalmente el resultado de la activación de los receptores de AMPA, a medidas
que el ataque se intensifica se evidencia una mayor participación del NMDA. Los
antagonistas del receptor de NMDA pueden reducir la intensidad y la duración de
la actividad. El antagonismo del receptor de AMPA normalmente previene el
inicio del ataque. Esto sugiere que la epilepsia depende de la interacción del
AMPA sináptico y los receptores de NMDA. De
igual manera su deficiencia pudiera ser una condición de los retrasos y
dificultades en el aprendizaje y la memoria.
El glutamato y el aspartato son
aminoácidos no escenciales que no pueden
atravesar la barrera hematoencefálica por consiguiente no llegan al cerebro a
través del torrente sanguíneo. Son sintetizados a partir de la glucosa y de
algunos precursores. La síntesis y el
metabolismo del glutamato y del aspartato dependen más de la interacción entre
las terminales nerviosas y las células gliales. Las vesículas sinápticas
acumulan de manera activa glutamato a través de procesos que dependen del ATP y
del Mg2+. El glutamato liberado como neurotransmisor es absorbido por la célula
glial la cual con gasto de ATP se incorpora el nitrógeno, y con la intervención
de la glutamina sintetasa se forma glutamina la cual es liberada por la
célula glial y es capturada por la neurona por difusión a
través de la membrana celular con facilidad se produce y libera glutámico por
acción de la glutaminasa.
La liberación de estos
neurotransmisores es dependiente del calcio y su inactivación es sodio
dependiente.
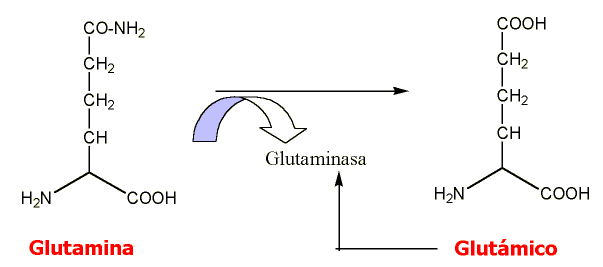
Figura 2: Autorregulación del glutámico. Tomado de Gómez-Jarabo, G. (ed.): "Farmacología de la conducta: Manual Básico para Psicoterapeutas y Clínicos"
Estos aminoácidos actúan sobre los
tres receptores de la membrana postsináptica: la mayoría de los receptores de
glutamato son ionotrópico; eso quiere decir el lugar donde se enlazan los
agonistas y el canal iónico asociado, se encuentran incorporado dentro del
mismo complejo macromolecular. Los agonistas actúan para aumentar la
probabilidad de que el canal iónico se abra. El NMDA, el AMPA y el Kainato (Ka)
como receptores de glutamato hacen parte de la familia de canales iónicos de
puertos de enlace, donde se incluyen los receptores nicotínico de la acetil
colina, los receptores del ácido
g-aminobutíricoA (GABA A), los receptores inhibitorios de la glicina y los
receptores de la 5-hidroxitriptamina3 (5HT3), entre otros.
La capacidad que tienen el glutamato y
la glicina para activar los receptores de NMDA es influenciado por el ph
extracelular y por el estado de fosforilación del receptor. Entre mas alcalino
sea el ph, mas alta será la frecuencia de apertura del canal ante la presencia
de una cantidad de agonistas determinado.
Los receptores metabotrópicos de
glutamato reciben este nombre por que son enlazados por proteínas G a encimas
citoplasmáticas. La activación de estos receptores produce en diferentes tipos
de células, un aumento en la concentración de calcio Ca+ intracelular mediado
por hidrólisis fosfoinositada, liberación de ácido araquidónico, mediado por la activación de la fosfolipasa
D, é incremento ó disminuciones en los niveles de AMPc.
Los receptores metabotrópicos producen
una variedad de efectos en la transmisión sináptica exitatoria é inhibitoria
debido a que el receptor está asociado a múltiples enzimas efectoras.
2.1.2.
HISTAMINA
La histamina es una molécula hidrófila
compuesta de un anillo imidazol y un grupo amino unidos por dos grupos
metileno. Está distribuida en todo el reino animal y forma parte de muchos venenos, bacterias y
plantas. Las concentraciones en plasma y otros líquidos corporales son pequeñas
pero en el líquido cefalorraquídeo en humano se halla en cantidades
importantes. La célula cebada es el sitio predominante de almacenamiento de la
histamina en casi todos los tejidos; la concentración de esta sustancia es
grande en tejidos que contienen gran número de células cebadas como piel y
mucosa del árbol bronquial y de las vías intestinales.
2.1.2.1. SINTESIS ALMACENAMIENTO Y
DEGRADACION
La histamina ingerida ó formada por
bacterias de las vias gastrointestinales
es metabolizada y eliminada rápidamente en la orina. El sitio principal
de depósito además de las células cebadas de los tejidos, los basófilos de la
sangre.
Hay dos vias importantes de
metabolismo de la histamina, en seres
humanos la más importante es la metilación del anillo, y es catalizada por la
enzima histamina-N-metiltransferasa. Gran parte del producto N-metilhistamina,
es transformada por la monooxidasa (MAO) a ácido N-metilimidazol acético; dicha
reacción puede ser bloqueada por los inhibidores de la MAO. En la otra vía, la
histamina es sometida a desaminación oxidativa, que es catalizada por la
diaminooxidasa DAO, enzima inespecífica. Los productos son el ácido imidazol
acético, y al final su ribóxido. Los metabolitos son excretados en la orina.
2.1.2.2. FUNCIONES DE LA HISTAMINA
ENDOGENA.
La histamina desempeña actividades
fisiológicas importantes. Debido a que es uno de los mediadores preformados
almacenados en la célula cebada su liberación como consecuencia de la
interacción del antígeno con los anticuerpos IgE en la superficie de dicha
célula interviene en las respuestas de hipersensibilidad inmediata y alérgica. Las acciones de la histamina en el
músculo liso de los bronquios y de vasos sanguíneos explican en parte la
reacción alérgica. La histamina interviene en la regulación de la secreción del
ácido gástrico y mas recientemente se ha identificado su función como
neurotransmisor del sistema nervioso central. Hay pruebas abundantes de que la
histamina es un neurotransmisor del sistema nervioso central. En este sistema
están distribuido de manera irregular la histamina, histidina descarboxilasa, las enzimas que catalizan la degradación de
la histamina y estas se hallan concentradas en las fracciones simpaticosómica
de homogeneizados cerebrales. Los receptores de H1 se encuentran distribuidos
en todo el sistema nervioso central y se concentran en el hipotálamo. La
histamina intensifica el estado de vigilia (Monti 1993) por medio de los
receptores H1 lo cual explica la capacidad sedante de los antihistamínicos
clásicos. La histamina actúa en los
receptores H1 é inhibe el apetito (Ookuma y cols. 1993). Las neuronas que
contienen histamina pueden participar en la regulación de la ingestión de
líquidos, temperatura corporal, y secreción de hormona antidiurética, así como
en el control de la presión arterial y percepción del dolor.
2.2.
AMINOACIDOS INHIBITORIOS.
2.2.1.
GABA
Los principales neurotransmisores
inhibitorios del SNC son los aminoácidos GABA, los cuales se encuentran en todo
el SNC y la glicina que predomina en la médula espinal.
El GABA se encuentra en
concentraciones 1000 veces mayores que los neurotransmisores monoaminérgicos
clásicos. Las neuronas GABAérgicas se encuentran abundantemente en el sistema
nervioso especialmente a nivel del encéfalo, a nivel de la médula espinal se
encuentran representado por la glicina, la cual actúa como un neurotransmisor
inhibitorio en la médula espinal debido a que las interneuronas de Renshaw son
glicinérgicas, recogen la información que proyectan colateralmente las
motoneuronas espinales, organizan una vía de retroalimentación que inhibe a las
mismas y regulan la vía común final.
El
GABA está presente en el cerebelo, donde las células de purkinje que recogen las
principales aferencias desde el bulbo actúan liberando GABA al tálamo é
hipotálamo, núcleos grises basales y al córtex
cerebral especialmente en la capa cuarta. De igual forma se encuentra presente
en la sustancia negra, la cual contiene gran cantidad de neuronas
dopaminérgicas. El contenido de GABA y sus sistemas enzimáticos en la sustancia
negra permiten entender que la regulación de la actividad dopaminérgica de la
sustancia negra sobre el estriado depende de la intervención del GABA.
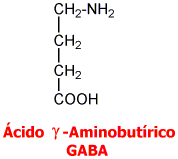
Figura3: Fórmula del GABA
El GABA se sintetiza a partir del
ácido glutámico a través de la intervención específica del
ácido-glutámico-descarboxilasa (GAD) un sistema enzimático dependiente del
fosfato de piridoxal (pp), el cual es exclusivo de los mamíferos y se encuentra sólo en el sistema
nervioso. En la biosíntesis desde el a-cetoglutárico la acción del
aspartatoaminotransferasa produce glutámico que por la acción de la GAD ante la
presencia de pp, da ácido g-aminobutírico (GABA) como producto final. Su degradación
enzimática se produce mediante la intervención de la g-transaminasa (GABA T),
el cual transporta al grupo amino al
a-cetoglutárico, finalmente se oxida al ácido succínico como producto final.
La liberación del GABA y de la glicina
es calcio-dependiente, la recaptura es
el medio de inactivación, las células gliales absorben el GABA, además
participan en su depósito mediante la formación de glutamina. De igual forma
participan en su catabolización mediante la inclusión en el proceso energético
de las mitocondrias gliales el cual se conoce como el cortocircuito GABA, esta
es la forma como la glia participa en la regulación de uno de los
neurotransmisores de mayor trascendencia en los procesos de regulación y en la
capacidad funcional del sistema nervioso.
2.2.2.
GLICINA.
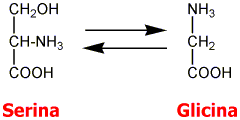
Figura 3: Formación de
glicina. Tomado de Gómez-Jarabo, G. (ed.): "Farmacología de la conducta:
Manual Básico para Psicoterapeutas y Clínicos
La glicina se forma a partir de la
serina, aminoácido que se forma a partir del ácido pirúvico el precursor
inmediato es la serina que se convierte en glicina por la actividad de la
encima serina hidroximetiltransferasa (SHMT) la liberación de la serina depende
del Ca2+ se han encontrado receptores postsinapticos específicos. La glicina es
reconocida como uno de los neurotransmisores principales del sistema nervios
central de vertebrados especialmente a nivel de la médula espinal, inhibe el
disparo neuronal abriendo los canales de Cl-. Entre sus antagonistas se
encuentra la estricnina, la cual bloquea la actividad de la glicina impidiendo
la relajación de las estructuras esqueléticas. La deficiencia de la glicina
tiene efectos convulsivantes.
Los aminoácidos que activan el
receptor de la glicina son: la b-alanina, taurina, L-alanina, L-serina y
prolina.
Las alteraciones de las neuronas
productoras de aminoácidos GABA pueden conducir a trastornos del movimiento, así como también a problemas de ansiedad
y epilepsia.
2.2.3.
TAURINA.
La taurina es un aminoácido neutro en
cuya composición entra a formar parte el azufre. Es uno de los aminoácidos más
abundantes en el músculo, las plaquetas y el sistema nervioso en desarrollo. Se
sintetiza a partir de la cisteína, el cual es otro aminoácido azufrado, por
acción de una decarboxilasa similar a la GAD.
Parece que su papel inhibitorio se
reduce a una actuación en la médula espinal, como la glicina. En comparación
con la intensa actividad del GABA en el cerebro, la taurina solo tiene una
débil acción depresora.
La taurina comprende más del 50% de
los aminoácidos libres del corazón. En las enfermedades oculares, se sabe que
existen altas concentraciones de taurina en la retina del ojo donde parece que funciona como buffer celular
protegiendo a las células retinales de los efectos nocivos de la luz
ultravioleta y las sustancias tóxicas. La taurina también tiene un papel clave
en la acción digestiva de la bilis. Actúa regulando las sales y el agua dentro
de la célula estabilizando la membrana celular. La función más importante de la taurina es
estabilizar la membrana de las células nerviosas. Si la membrana de la célula
está eléctricamente inestable, la célula nerviosa puede disparar demasiado
rápido y erráticamente, lo cual puede ocasionar alguna forma de epilepsia. Otra
teoría de la epilepsia sostiene que es causada por cantidades anormales de
ácido glutámico en el cerebro. Deacuerdo a esto la taurina trabajaría
estabilizando los niveles de ácido glutámico.
3.
MONOAMINAS
El sistema monoaminérgico se origina
en grupos de neuronas que se encuentran ubicadas en el tronco cerebral, luego
se proyectan a distintas áreas del
SNC. En todas sus ubicaciones se une a
un gran número de receptores, lo cual hace que su acción sea compleja.
Constituyen el grupo principal de
neurotransmisores del sistema nervioso. La diferencia de estas sustancias es la
presencia de un grupo amino
(-NH2) de ahí que se denominan
monoaminas, proceden de aminoácidos precursores
y forman dos grupos: las catecolaminas, las cuales se derivan de la
fenilalanina, en la biosíntesis nerviosa acortan el camino iniciándolo en la
paratirosina; y las indolaminas que derivan del triptofano.
Las catecolaminas incluyen la
dopamina, la adrenalina y la noradrenalina y las indolaminas el neurotransmisor
es la serotonina. Tienen una ubicación troncoencefálica y también cerebral,
interviniendo en la modulación funcional de grandes regiones cerebrales como los núcleos grises
basales, el sistema límbico y la corteza. La modificación de sus niveles se
encuentra relacionada con las alteraciones expresivas y las expresiones
psicóticas.
3.1.1.
DOPAMINA
Se puede llegar a considerar que la
dopamina es la monamina más importante por su localización mas superior que la
noradrenalina a nivel del encéfalo por lo tanto está más comprometida en el
comportamiento del individuo. Las neuronas que contienen dopamina pueden
clasificarse en tres grupos: mesocorticales, nigroestriadas y tuberhipofisales.
El principal tracto dopaminérgico del cerebro se origina en la sustancia negra
y envía sus axones al núcleo caudado y
al cuerpo estriado; en el cuerpo estríado se encuentra el 80% de la
dopamina presente en el cerebro. Las neuronas ubicadas medialmente a la
sustancia negra, proporcionan una inervación difusa al cerebro anterior, incluyendo el córtex frontal, el cingulado
y el tubérculo olfatorio. Las neuronas que contienen dopamina en los
núcleos arcuatos y paraventricular del hipotálamo, inervan el lóbulo intermedio de la pituitaria y la eminencia media. Además
de estas vías principales se han encontrado interneuronas en el bulbo olfatorio y en la retina neural
que contienen dopamina.
El núcleo rojo, los núcleos
cuneiformes, la sustancia negra y las áreas tegmentales son estructuras
dopaminérgicas y constituyen tres fascículos de gran importancia en el
encéfalo: el fascículo negroestriado el
cual tiene gran cantidad de proyección hacia los núcleos grises basales; el fascículo mesolímbico que se
proyecta hacia el sistema límbico y
el fascículo mesocortical que se proyecta además de las estructuras internas de
la corteza, la estructura prefrontal. Teniendo en cuenta la función de las
estructuras mencionadas (control y regulación del movimiento, expresión de los
estados afectivos, capacidad de proposición y juicio) debe considerarse que la
dopamina está involucrada en cada una de
esas funciones.
A nivel del tálamo é hipotálamo
también se encuentra pero de manera difusa por eso se consideran proyecciones
inespecíficas cuya función está relacionada con la regulación de la economía,
metabolismo orgánico mediante la secreción de factores de regulación de las hormonas tiroideas.
Existen aproximadamente 500.000
células dopaminérgicas en el mesencéfalo del adulto joven la mayoría de las
cuales se encuentran en la pars compacta de la sustancia negra. Estas células
contienen neuromelanina y fabrican la dopamina. Junto con las células pigmentadas del área adyacente del área tegmental
ventral, proporcionan toda la inervación tegmental del encéfalo. El sistema nigroestratial participa en la
planeación y ejecución automática de los movimientos aprendidos y se considera
que la vía dopaminérgica al estriado posee una actividad moduladora de este
proceso. De esta manera la población
neuronal de la sustancia negra influencia la producción motora de los ganglios basales. La pars
compacta envía un estímulo exitatorio de movimiento al tálamo y a la corteza.
El sistema límbico formado por porciones del cerebro de precoz desarrollo
filogenético y ontogénico, situadas en la porción medial del hemisferio. El
lóbulo límbico está conformado por las estructuras que configuran la formación
del hipocampo, la corteza parahipocampal y el núcleo amigdaloide con sus
conexiones. Estos sistemas relacionan al lóbulo límbico con el sistema nervioso
autónomo en el área hipotalámica (regula las respuestas automáticas ante las
emociones). Por otro lado las emociones tienen relación con la voluntad
mediante el núcleo acumbens. Está demostrado que este sistema mesolímbico
utiliza Dopamina. El aumento de la dopamina en este sistema estimula el núcleo
acumbens y la activación de éste núcleo con ese neurotransmisor se ha asociado
a esquizofrenia y alucinaciones.
En la hipófisis la Dopamina inhibe la
liberación de hormonas especialmente la prolactina. En el hipotálamo se produce
un factor inhibitorio que impide la liberación de prolactina en el hipotálamo.
Este factor viaja a la hipófisis a través del sistema porta. Este factor
inhibidor es la Dopamina. Se ha visto como un aumento de la Dopamina disminuye
la liberación de prolactina. Mientras que una disminución de la Dopamina
aumenta la liberación de prolactina.
Los receptores de la dopamina son:
Tabla
1: receptores de la Dopamina
|
RECEPTOR |
MECANISMO
DE ACCION |
|
D1 |
Aumenta el AMP cíclico. |
|
D2 |
Disminuye el AMP cíclico |
|
D3 |
Disminuye el AMP cíclico |
|
D4 |
Disminuye el AMP cíclico |
|
D5 |
Aumenta el AMP cíclico |
Los receptores dopaminérgicos D1 se
encuentran en la zona compacta de la
sustancia nigra y presinàptica en los axones estratiales que vienen de las neuronas corticales y de las células
dopaminérgicas de la sustancia nigra. Los receptores D2 se localizan en la
membrana postsináptica de las neuronas estratiales y en la membrana
presinàptica de los axones de la sustancia nigra que provienen de las neuronas
ubicadas en los ganglios basales. Se puede afirmar que en el sistema nigro
estratial el principal receptor que está presente es el D2.
3.1.1.1.
METABOLISMO Y DISTRIBUCION DE LA DOPAMINA.
La biosíntesis de la dopamina está
relacionada a la de la noradrenalina su degradación tiene los mismos sistemas
enzimáticos pero se diferencia dependiendo de cual sea el primer factor
enzimático que actúe.
La síntesis de dopamina tiene tres
pasos básicamente:
La fenilalanina es convertida en
tirosina por la enzima fenilalanina hidroxilasa. La tirosina se convierte en
DOPA (Dihidroxifenilalanina) por la enzima tiroxina hidroxilasa. La DOPA se
convierte en dopamina por la enzima Dopa descarboxilasa.
Una parte de la Dopamina liberada es
recaptada por la neurona sin sufrir ninguna modificación. El remanente de la Dopamina
queda disponible para actuar sobre los receptores y autoreceptores. La Dopamina
se metaboliza en sangre, hígado y riñones por la monoaminooxidasa (MAO) y la
catecol-o-metiltransferasa en los compuestos inactivos: ácido homovanílico (HVA)
y ácido 3,4-dihidrofenilacético. Una parte de la dopamina se metaboliza a
norepinefrina dentro las terminales nerviosas adrenérgicas.
3.1.1.2.
IMPLICACIONES FUNCIONALES Y PATOLOGIAS RELACIONADAS
Actualmente se aceptan dos receptores
dopaminérgicos centrales: D1 y D2 y otros dos receptores
periféricos DA1 y DA2. Los
receptores D1 son postsinapticos y los D2 son postsinapticos y
presinápticos. Los primeros utilizan el AMPc para actuar y como consecuencia
inmediata se activa la adenilciclasa, pero los segundos inhiben la actividad de
la adenilciclasa. Por consiguiente su alteración funcional y la actividad de
sus agonistas y antagonistas van a depender de la densidad de receptores de uno
u otro tipo que se presenten en las estructuras encefálicas y del umbral de
sensibilidad que presentan a la dopamina. Parece que los receptores D1
se encuentran en
mayor concentración en las proyecciones nigroestriada y mesolímbicas y que los D2
se encuentran en
las proyecciones mesocorticales.
La sustancia negra tiene proyecciones
dopaminérgicas sobre el núcleo caudado y el putamen, éstos a través del putamen
regulan la actividad motora, al parecer las neuronas del cuerpo estríado están
reguladas por la acetil colina, la cual tiene una función exitatoria, la
dopamina que tiene una función inhibitoria al estar regulada por el GABA, y
disminuir sus niveles se producen
efectos motores extapiramidales resultantes de una hiperactividad colinérgica.
3.2.
ADRENALINA –NORADRENALINA
La adrenalina a pesar de ser
considerado como un neurotransmisor, su acción es relegada por la acción de la
noradrenalina. Esto es debido a que la adrenalina secretada por las glándulas
suprarrenales por acción simpática, tiene
un efecto generalizado igual al la acción de la noradrenalina producida por la
neurona postsináptica de una vía autónoma.
La noradrenalina es por
consiguiente la catecolamina que se utiliza como neurotransmisor a nivel del
sistema nervioso central. El conglomerado de neuronas adrenérgicas se
encuentran en el locus cereleus, estructura identificada a nivel del tronco
cerebral.
Desde el locus cereleus
y otras áreas noradrenérgicas más inferiores como el núcleo del tracto
solitario ó los núcleos reticulares laterales, surgen dos fascículos de
proyección ascendente: el fascículo noradrenérgico dorsal y el fascículo noradrenérgico ventral. Ambos fascículos tienen implicación en la
actividad cortico-subcortical por su proyección al córtex, sistema límbico,
diencéfalo, tálamo é hipotálamo. De
igual manera se proyectan hacia la formación reticular de la médula cuya
función principal es la de regular los
niveles de vigilancia, particularmente en la actividad mínima de la vigilia,
definiendo los niveles de atención,
emoción, é hiperexitabilidad, por lo tanto se considera que juega un papel
importante en la regulación de la conducta.
3.2.1. METABOLISMO Y DISTRIBUCION
La dopa decarboxilasa es
una encima piridoxinodependiente que cataliza la eliminación del grupo
carboxilo de la dopa para formar dopamina. La dopa decarboxilasa puede también
decarboxilar el 5 dihidroxitriptófano, precusor de la serotonina. La
dopadecarboxilasa se halla distribuida en todo el cuerpo por consiguiente se puede encontrar en neuronas que contienen catecolaminas y
serotonina y en tejidos no neurales como riñones y vasos sanguíneo.
Cuando un potencial de
acción alcanza el terminal nervioso, se abren los canales Ca2+, permitiendo un
flujo de catión en el terminal; el incremento del Ca2+ intracelular promueve la
fusión de de vesículas con la membrana neuronal. Las vesículas descargan sus
contenidos solubles, incluyendo noradrenalina, ATP y DBH dentro del espacio
extraneuronal. La liberación desde las neuronas simpáticas podría ser el origen
de algunas de las DBH encontradas en el plasma y en el líquido cerebroespinal
de animales y humanos.
Hay mecanismos
reguladores que operan eficientemente para modular la síntesis de
catecolaminas. Un proceso de larga duración que afecta la síntesis de
catecolaminas trae consigo alteraciones en las concentraciones de TH y DBH
presentes en las terminales nerviosas. Cuando el nivel de actividad neuronal
simpática aumenta por un largo período de tiempo las concentraciones de ARNm
que codifican TH y DBH se incrementan en la pericarión neuronal.
La monoamino oxidasa MAO
y la catecol- oxi-metiltransferasa COMT son las enzimas encargadas de la
inactivación de las catecolaminas. Estas se encuentran distribuídas por todo el
cuerpo. La MAO es una encima que contiene flavina se encuentra localizada sobre
la membrana exterior de la mitocondria. Esta encima oxida a las catecolaminas a
sus aldehídos correspondientes; estos pueden convertirse en aldehído
deshidrogenasa en ácidos, ó por aldehídos reductasa para formar glicoles. Debido
a su ubicación intracelular, la MAO desempeña un papel estratégico en la inactivación
de las catecolaminas que se encuentran libremente en la terminal nerviosa y no
están protegidos por la vesícula de almacenamiento. Deacuerdo con esto las
drogas que interfieren con el almacenamiento vesicular como la reserpina,
anfetaminas que desplazan a las catecolaminas de las vesículas provocan un
aumento significativo de los metabolitos deaminados.
Los cuerpos celulares de
las neuronas noradrenérgicas se encuentran ubicados en la médula oblongada, el
puente y el cerebro medio, anatómicamente se consideran parte de la formación
reticular.
La noradrenalina se
biosintetiza en las terminaciones sinápticas
a partir del aminoácido tirosina por acción de la tirosina hidroxilasa,
produciéndose la dopa la cual mediante la acción de la dopa decarboxilasa se
convierte en dopamina (DA) la primera de las catecolaminas. La dopamina por
hidroxilación con la b-hidroxi-dopamina se transforma en noradrenalina (NA),
que es la segunda de las catecolaminas. Finalmente, la NA por una metilación
con la feniletanolamina N-metiltransferasa (PNMT), se convierte en adrenalina
(A).
La diferenciación de las
neuronas por su actividad dopaminérgica, noradrenérgica ó adrenérgica, se basa
en primer lugar de una actividad enzimática tirosina hidroxilasa y en segundo
lugar en la ausencia de dopamina b-hidroxilasa para las neuronas
dopaminérgicas, ó en ausencia de actividad PNMT para las neuronas
noradrenérgicas.
En relación al
almacenamiento en el botón terminal, las catecolaminas se almacenan conjugadas
a una proteína ácida, la cromogranina que protege al neurotransmisor de la
acción de enzimas degradantes, pero es fácilmente reparable y separable por la
intervención del ATP.
La liberación de NA se
debe al flujo de iones de Ca2+ que acompañan al potencial de acción, de igual
manera con la Ach, este es el efecto utilizado especialmente por las
anfetaminas, para un mayor efecto de activación postsináptica.
Una vez liberada la
catecolamina, el principal mecanismo de desactivación es la recaptación. En este mecanismo
participa la bomba de Na+, que se denomina bomba de amina. En este fenómeno los
fármacos tricíclicos inhiben la recaptación, por lo tanto su efecto es
potenciar las catecolaminas. Este es el valor terapéutico de los antidepresivos
tricíclicos.
La acción
enzimática también constituye una parte
importante en la inactivación de las catecolaminas. Los sistemas implicados son
MAO Y COMT. Ellos actúan de manera sucesiva y oxidan al grupo amino é
incorporan un grupo metilo respectivamente. De esta manera la inhibición de los
sistemas enzimáticos principalmente de la MAO, da lugar a un grupo denominado
inhibidores de la MAO (IMAOs).
3.2.2. RECEPTORES DE LAS CATECOLAMINAS.
3.2.2.1. AUTORECEPTORES O PRERECEPTORES.
Los autoreceptores que
se encuentran en cualquier neurona responden a las moléculas transmisoras
liberadas por la misma neurona. En el terminal nervioso responden a las
moléculas transmisoras liberadas en el espacio sináptico, sobre el cuerpo
celular responderán a las moléculas transmisoras liberadas por las dendritas.
Desde el punto de vista funcional los autoreceptores regulan la liberación de
neurotransmisores.
3.2.2.2. RECEPTORES POSTSINAPTICOS.
Los efectos de la
dopamina están mediados a través de la interacción con los receptores del tipo D1
(D1 Y D5) y D2 (D2, D3 y D4) mientras que los efectos de la adrenalina y la
noradrenalina están mediados por los receptores a-adrenérgicos (a1 y a2) y a
través de los receptores b-adrenérgicos (b1 y b2).
La adrenalina y la noradrenalina actúan sobre los receptores a y
b. el antagonista receptor, b-adrenérgico propanolol está esencialmente
inactivo en los receptores. El antagonista receptor a-adrenérgico pentolamina
es muy débil en los receptores b. De los receptores b los b1 adrenérgicos, son
los que predominan en el corazón, y en el córtex cerebral, mientras que los
receptores b2 adrenérgicos predominan en el pulmón y en el cerebelo, sin
embargo en muchas estructuras los receptores b1 y b2-adrenérgicos, coexisten en
el mismo tejido. El cerebro contiene
receptores b1 y b2. Se han identificado un tercer tipo de receptores en el
tejido adiposo marrón presente en los roedores y en el los humanos recién
nacidos.
3.2.2.2.1. RECEPTORES a-Adrenérgicos.
Algunos tejidos poseen
solamente receptores a1, otros poseen solamente receptores a2 y otros poseen la
combinación de ambos receptores. Las consecuencias fisiológicas de ambos
receptores en el cerebro no están claras actualmente.
3.2.2.2.2. RECEPTORES b Adrenérgicos.
La noradrenalina tiene
escaso efecto sobre los receptores b2 adrenérgicos. Es difícil encontrar un
agonista puro para los receptores b por lo tanto lo que se observa como
parámetro de valoración terapéutica es la relación existente entre los
receptores b1 y b2.
4.1. SEROTONINA
A principios del siglo
veinte, las plaquetas fueron identificadas como la fuente de la
Indolalquilamina 5-hidroxitriptamina (5-HT; serotonina), a mediados de la
década de los cuarenta Page y colaboradores aislaron y caracterizaron esta
sustancia tónica del suero (serum; desde aquí, serotonina).
La combinación del grupo
hidroxilo en la posición 5 del núcleo indol, y una amina nitrogenada primaria
actuando como aceptador de un protón del Ph
fisiológico, hace de la 5-HT una sustancia hidrofílica. Por consiguiente
no traspasa la barrera hematoencefálica con facilidad. Su descubrimiento en el
cerebro en 1953 por Twarog y Page indicó que la 5-HT estaba siendo sintetizada
en el cerebro. La observación simultánea de que la droga sicodélica Dietilamida
del ácido lisérgico (LSD) antagoniza una respuesta producida por el 5HT,
confirmó la idea de que la 5-HT era un producto de nuestro cerebro y tiene
importante efectos conductuales.
No todas las células que
contienen 5-HT la sintetizan. Las plaquetas por un mecanismo de transporte
activo que se encuentra en su membrana acumulan 5-HT. La síntesis se inicia con
el transporte facilitado de un aminoácido el L-triptofano, de la sangre hasta
el cerebro. Otros aminoácidos neutros como fenilalanina, leucina, metionina)
son transportados dentro del cerebro por el mismo mensajero.
Las neuronas
serotoninérgicas contienen la enzima triptofano-hidroxilasa, que convierte el
triptofano en 5-hidroxitriptófano (5-HTP) su distribución en el cerebro es
similar a la de 5-HT.
Otra enzima implicada en
la síntesis de la serotonina es el decarboxilasa de los aminoácidos L-aromático
(aminoácido decarboxilasa: AADC) el cual convierte al 5-HTP en 5-HT. Esta
enzima está presente no solo en las neuronas serotoninérgicas sino que se
encuentran presentes en las neuronas catecolaminérgicas, en las cuales
convierte el 3,4-dihidroxifenilalanina (DOPA) en dopamina.
En 1964 Dalhstrom y
Fuxe, usando la técnica de histofluorescencia de Falck y Hallarp, encontró que
la mayoría de los cuerpos serotoninérgicos se encontraban en el núcleo de Raphé.
Estos investigadores describieron nueve grupos de cuerpos celulares que
contienen serotonina, a los cuales ellos desginaron desde B1 hasta B9 y estos se corresponden en su
gran mayoría con los núcleos de Raphé.
El grupo mayor de
células serotoninérgica es el grupo B7
contiguo al grupo B6, el cual es más pequeño, estos dos grupos se consideran el
núcleo dorsal del núcleo de Raphé, siendo B6 la parte más caudal del núcleo.
Otro grupo prominente de células las B8 que corresponden al núcleo medio de
Raphé, El grupo B9 que parte del tegmento ventrolateral del puente y del
cerebro medio. Las proyecciones serotoninérgicas ascendentes, que inervan al córtex y otras regiones del cerebro anterior, vienen
desde el Raphé dorsal, medio y el grupo celular B9. El resto de grupos
celulares de B1 a B5 contienen un número bajo de células serotoninérgicas.
Los núcleos de Raphé
dorsal y medial dan salida a axones que forman vias separadas para distintas regiones cerebrales.
Algunas estructuras
funcionalmente parecidas en el cerebro son inervadas por el mismo grupo de
células serotoninérgicas. Por ejemplo el hipocampo y el séptum (estructuras del
sistema límbico) parecen que están inervadas por células del núcleo de Raphé
medial, el estriado y la sustancia negra (estructuras de los ganglios basales
relacionados con el control de la actividad motora) son inervadas por el grupo
de células del núcleo Raphé dorsal. Algunas células dentro del núcleo de Raphé
se organizan de manera particular y mandan sus axones a regiones específicas
del cerebro como por ejemplo a la corteza frontal que recibe inervación de
subregiones rostrales y ventrales del núcleo de Raphé. De la misma forma como
estructuras funcionalmente parecidas son inervadas por grupos de neuronas, también
pueden ser inervadas por las mismas neuronas de manera individual.
La síntesis de 5-HT
puede aumentar de considerablemente bajo condiciones que requieren un
suministro continuo de neurotransmisor. La plasticidad es un concepto muy
importante en la neurobiología. Es la capacidad de los sistemas neuronales para
ajustarse a demandas a corto y /o largo plazo sobre su actividad ó
funcionamiento. Muchos procesos como el aumento de la capacidad de síntesis del
neurotransmisor y liberación en respuesta a un incremento de la actividad
neuronal, contribuyen con el mecanismo de plasticidad cerebral.
4.1.1. IMPLICACIONES FUNCIONALES DE LA SEROTONIa
Los receptores 5-HT1A están presente en alta
densidad en el hipocampo, séptum, amigdala, hipotálamo y neocórtex.
La serotonina está entre
los muchos neurotransmisores que participan en el control hipotalámico, de la
secreción pituitaria, especialmente en la regulación de la prolactina,
adrenocorticotropina (ACTH) y hormona del crecimiento. La medida de estas
reacciones endocrinas en el cerebro, proporciona uno de los pocos métodos
actualmente disponibles para evaluar dicha función en humanos.
La investigación en
gatos, ha implicado a la serotonina en el sueño y en el estado de activación
(arousal). Las neuronas seratoninérgicas en el núcleo de Raphé dorsal, muestran
un cambio en la actividad a lo largo del ciclo vigilia-sueño-activación. Bajo
condiciones de vigilia tranquila, las neuronas seratoninérgicas tienen una
actividad lenta, siguiendo las manecillas del reloj mostrando una disminución
gradual a medidas que el animal se va volviendo somnoliento y cae en sueño de
onda lenta. Durante el sueño REM
(movimiento rápido de los ojos), la actividad de las neuronas cesa. En
respuesta a un estímulo activado la tasa de disparo de estas neuronas aumenta.
Un estímulo auditivo (golpe) visual (destello) produce una excitación de las
neuronas seratoninérgicas del Raphé dorsal, seguidas por una inhibición.
Exponiendo al mismo animal a estresares ambientales como un fuerte golpe ó la
visión de un perro, aunque produce la activación simpática fuerte y una
reacción conductual típica no altera la tasa de disparo de estas neuronas
seratoninérgicas. Esto debido a que la actividad tónica de estas neuronas
parece variar de forma general y no asociado
con un estado conductual específico. Jacobs y sus colaboradores han
propuesto que el papel de las neuronas seratoninérgicas central es coordinar la
actividad del sistema nerviosa, fijar el tono de actividad en conjunción con el
nivel de activación del organismo. La serotonina también parece estar
implicada en la regulación del ritmo circadiano, el núcleo supraquiasmático del
hipotálamo genera ciclos
electrofisiológicos y metabólicos que repite cada 24 horas.
La investigación
neuroquímica, se ha focalizado en como afecta la alimentación a las
concentraciones de triptofano en el cerebro y en la disponibilidad de
serotonina, mientras que la investigación farmacológica ha estado basada en el
control del apetito por medio de medicamentos serotoninérgicos.
El papel de la serotonina (5HT) en el SNC, está completamente
ligado al de la NA, ya que interviene en
la regulación de la vigilancia, en el proceso activo del sueño, la
atención, los procesos motivacionales, y
en la regulación de los estados de ánimo. Por otro lado debemos tener presente
que el control de entrada del dolor parece depender de la liberación de
serotonina, que facilita la producción de endorfinas medulares.
Todo este papel se
realiza a través de una localización sucesiva de estructuras, de los núcleos de
Raphé. Las proyecciones de estos núcleos a través del fascículo medio del
telencéfalo, suelen ser inhibitorias, de ahí que la actividad de regulación de
las catecolaminas no se puede separar de la de la serotonina.
La destrucción de los
núcleos de Raphé, ó la administración de una sustancia como dihidroxitriptamina,
conduce a un incremento de la actividad nerviosa. Pero además también hay
situaciones en las que la serotonina en vez de inhibir, excita, demostrándose
esta acción con los efectos activadores autónomos y motores, y no se pueden
olvidar los efectos alucinógenos de los propios agonistas de la serotonina, los
cuales mediante una actuación sobre los receptores presinápticos, ofrecen una
consecuencia de hiperactividad típica de las alucinaciones táctiles y visuales.
La acetil colina Ach es
el neurotransmisor específico en la sinápsis del sistema nervioso somático
(SNS) y en las sinapsis ganglionares del sistema nervioso autónomo (SNA), así
como en los órganos diana de la división parasimpática. El que se haya
comprobado el papel exitatorio de la sinápsis colinérgica en la placa
neuromuscular y de su papel inhibitorio sobre la membrana de las fibras
musculares cardíacas comprueba la
consecuencia de la naturaleza de los canales iónicos controlados por los
receptores colinérgicos postsinápticos. En el músculo esquelético el control se
hace sobre los canales iónicos de sodio y en el músculo cardíaco sobre los
canales iónicos de potasio.
La acetil colina también
se encuentra ampliamente distribuída en el encéfalo y es un neurotransmisor
clave en la regulación de los niveles de
vigilia y en el funcionamiento de las grandes áreas de asociación.
5.1. METABOLISMO Y DISTRIBUCION
La síntesis de la acetil
colina se realiza en el botón terminal mediante la utilización de dos
sustancias precursoras, el acetato y la colina. La síntesis exige la
incorporación del acetato a la colina y la intervención del sistema enzimático
acetil-colina-transferasa (Chat), que a su vez necesita la presencia de una
coenzima, la coenzima –A, para transferir el acetato. En la síntesis, el
proceso fundamental se refiere a la acción de la Chat, que ante la presencia de
acetilcoenzima A y del aminoalcohol colina, deja libre la coenzima y da como resultado
el producto final de la reacción, que es el neurotransmisor acetilcolina.
En cuanto a su
degradación, el sistema enzimático
imprescindible para la catabolización, es la intervención de la
acetilcolinesterasa (AChE) postsináptica, que se une específicamente a la
acetil colina y la rompe en dos moléculas, liberando los propios precursores de
su síntesis.
El Ca++ es de gran importancia en la transmisión
colinérgica, se sabe que son necesarios cuatro iones de Ca++ para abrir una
vesícula colinérgica, por lo tanto es imprescindible mantener una alta
concentración de calcio extracelular para que la transmisión del impulso
nervioso termine con la liberación de la acetil colina. Por consiguiente la
eliminación del Ca++ extracelular ó el bloqueo de su acción por ejemplo con la
competencia del magnesio (Mg++) disminuyen
é incluso inhibe la liberación de la acetilcolina, como ocurre con algunos
venenos, y toxinas como la toxina botulínica.
En el tronco cerebral
responden a la acción colinérgica entre otros, los núcleos cocleares; los
centros respiratorios; muchos pares craneales aferentes; la propia formación
reticular que responde con activación en
una tercera parte de la misma y en una décima parte con inhibición; las
estructuras subtalámicas que son colinérgicas y responden con una activación
descendente y una inhibición ascendente; el núcleo cuneiforme y los núcleos
tegmentales son también colinérgicos y están implicados en los reflejos
condicionados y en las respuestas de orientación.
A nivel subcortical hay
que tener en cuenta el papel de los núcleos grises basales, aunque hay neuronas
que responden con activación y otras con inhibición.
El papel de la
acetilcolina también es importante en el diencéfalo. En el hipotálamo la
activación colinérgica puede producir la
hipotermia. También parece que la acción colinérgica produce la liberación de
neurohormonas, como la antidiurética y la oxitocina. En el tálamo la actividad
colinérgica es importante para la función del sistema talámico difuso y
consecuentemente en la regulación del
nivel de vigilancia de la corteza cerebral.
Con esta distribución de
la acetil colina en el sistema nervioso central, los efectos centrales de una
acción anticolinérgica producen síndromes característicos como pérdida de la
memoria y atención, habla confusa y ataxia, confusión y desorientación.
La organización del
sistema nervioso colinérgico se basó inicialmente en la actividad farmacológica
de dos alcaloides: la nicotina y la muscarina. No todos los receptores
nicotínicos son iguales los que se encuentran en la unión neuromuscular se
denominan N1, muestran selectividad por el feniltrimetalmonio como agonista.
Los agentes biscuaternarios siendo el decametonium el mas potente son
bloqueados preferentemente por el antagonista d-tubocurarina; y son bloqueados
irreversiblemente por las a-toxinas de las serpientes. Los receptores
nicotínicos en los ganglios, receptores N2, son estimulados preferentemente por
fenilpiperazina, bloqueados competitivamente por trimetapan, bloqueados por
agentes bicuaternarios, siendo el hexametonio el mas potente y son resistentes
a las a-toxinas de serpiente.
Los receptores
muscarínicos tienen también varios subtipos. El antagonista pirenzapina (PZ)
tiene mayor afinidad por un subtipo llamado M1, el cual se encuentra principalmente
en los tejidos neuronales. Otro antagonista, AFDX-116 tiene la mayor afinidad
por los receptores M2, predominantemente en el corazón de los mamíferos. Los
antagonistas piridina son relativamente selectivos para el M3 presente en el músculo
liso y glándulas mientras que la himbacina tiene afinidad por los receptores
M4.
En cuanto a los aspectos
funcionales de la neurotransmisión colinérgica,
los subtipos individuales de receptores tienen localizaciones anatómicas
discretas en el sistema nervioso periférico. Los receptores nicotínicos se
encuentran en los ganglios periféricos y en el músculo esquelético. En la
inervación del músculo esquelético, los receptores se congregan en la unión ó
en el área postsináptica de la placa terminal. En la denervación los receptores
se encuentran distribuídos a lo largo de la superficie del músculo. Los
receptores nicotínicos de los ganglios se encuentran en las neuronas
postsinápticas tanto en los ganglios simpáticos y para simpáticos y en la
glándula adrenal. Los receptores muscarínicos son responsables de la
neurotransmisión parasimpática postglanglionar. La sudoración y la
piloroerección son mediados por receptores muscarínicos también.
5.2. RECEPTORES COLINERGICOS AGONISTAS Y ANTAGONISTAS.
El receptor nicotínico
es una glucoproteína de las cuales dos son cadenas peptídicas, aunque son
homólogas no son equivalentes. Las subunidades son claves en la activación del
receptor y además tienen un funcionamiento sucesivo, es decir, la unión de la
acetil colina al radical de alta afinidad de una subunidad permite el acceso de
otra acetil colina a la segunda subunidad a.
Se abre la conductancia y aparece la consecuencia receptora.
El receptor muscarínico
da una respuesta más lenta pero sus efectos son más duraderos. Este receptor
necesita un segundo mensajero.
La información que
transporta una neurona va codificada en señales eléctricas que viajan a lo largo de su axón a las
terminales nerviosas. En las sinápsis a través de las hendiduras las señales
son transportadas por uno ó más mensajero. Algunos son metabolitos del interior
de la célula: los aminoácidos se polimerizan en proteínas, el glutamato y el
GABA actúan como sustratos en el metabolismo intermediario, y el ATP es el
medio principal de transferencia de la energía metabólica.
Las moléculas se
convierten en señales cuando se unen a proteínas receptoras en la membrana de
otra célula haciendo que cambie de forma.
Los mensajeros químicos
están empaquetados en vesículas en el interior de la neurona. Después de su
síntesis en el citoplasma, los transmisores de pequeñas moléculas son captados
y concentrados en vesículas, donde están protegidos de las enzimas de degradación
que mantienen un nivel constante de neurotransmisor.
Las terminaciones
nerviosas contienen una gran concentración
de vesículas sinápticas. Cómo este se está liberando continuamente gran
parte del neurotransmisor de pequeña molécula de la neurona se sintetizará en
las terminales.
Para comprender la
estrategia molecular de la transmisión química, se debe identificar el
contenido de las vesículas sinápticas. Excepto en algunas neuronas en las que el
neurotransmisor es liberado por moléculas transportadoras, solo las moléculas
alojadas en las vesículas puede ser liberada de la misma terminal neuronal.
No todas las moléculas liberadas por una neurona son mensajeros químicos: solo las que se unen a receptores adecuados y así inician los cambios de actividad de la célula postsináptica pueden considerarse transmisores. Es típico que las vesículas medien la liberación de un mensajero químico por exocitosis, pero en algunos casos los transmisores se liberan por otros mecanismos
Bradford, H.
F.
"Fundamentos de Neuroquímica". Ed. Labor, 1988.
Dennis, Rains. Principios de Neuropsicología
humana. Primera edición 2002. McgrawHill.
Gómez-Jarabo, G. (Ed.): "Farmacología de
la conducta: Manual Básico para Psicoterapeutas y Clínicos". Ed. Síntesis Psicología.
Goodman y Gilman (Eds.). Las bases farmacológicas
de la conducta. (9ª edición) (Vols. I y II).
McGraw-Hill-Interamericana. México, 1996.
Haines. Duane E, Principios de Neurociencia.
Segunda edición. Elservier Science. 2003.
Kandel,
Eric R.; Schwartz, J, Jessell, Thomas M. Principios
de Neurociencias. Cuarta edición 2000. McGraw – Hill. Interamericana.
Llinás,
Rodolfo. I OF THE VORTEX. From Neurons to Self. 2001. The MIT press.revista de
Neurología. ALLEGRI, R. F. La
corteza prefrontal en los mecanismos atencionales y la memoria. Año. 2001; Vol.32 (5).
Revista de Neurología. HERNÁNDEZ, S.
ET AL.
Contribución del cerebelo a los procesos cognitivos. Año. 2005; Vol. 40(Supl 1)
Siegel, G. J.; Agranoff, B.W.; Wayne, R.; Molinoff, P.B. (eds.): "Basic Neurochemistry" 5th Edition. Raven Press,
Serratrice.
G, Habib. M, Escritura
y Cerebro Mecanismos Neurofisiològicos. Masson. 1997
CUESTIONARIO.
Cuestionario
de escogencia múltiple con única respuesta. Escoja la respuesta verdadera.
a. a
su importancia para el tratamiento y prevención de las enfermedades
cerebrovasculares.
b. a
su importancia para el tratamiento y prevención de las enfermedades
circulatorias.
c. la
importancia de conocer las concentraciones del Ca++
d. la
necesidad de continuar la exploración sobre el tema.
a. el
neurotransmisor sea depositado nuevamente en el espacio presinàptico.
b. los
transportadores de membrana entren en reposo
c. se
reinicie el proceso.
d. aumente
la conducción.
a. la
constitución del núcleo y la velocidad de conducción
b. presencia
de precursores y activación de sistemas enzimáticos.
c. la
concentración de los neurotransmisores y su conducción.
d. La
concentración de los neurotransmisores.
a. el daño obedece en parte a la acidosis de las células gliales y
liberación de radicales libres.
a. dejar
para que mediante mecanismos neuronales se genere su síntesis.
b. estimular
su síntesis a través de mecanismos secundarios.
c. se
recomienda la ingesta de calcio.
d. Estimular
la síntesis a partir de la glucosa que se encuentra en el cerebro.
a y b
c y d
b y c
a y c
a y d
b y c
c y d
a y c
a y b
b y c
c y d
b y d
a y b
b y d
a y c
b y d
a y d
b y c
c y d
a y c
1.
b y c
3.
c y d
a y c
d y b
a y b
d y c
a y d
b y c
a y c
d y b
a. la
dopamina no guarda relación con respuestas del sistema nervioso autónomo.
b. el
aumento de la dopamina, estimula al núcleo acumbens.
c. la
activación del núcleo acumben por la dopamina se ha asociado a trastornos
mentales como la esquizofrenia y las alucinaciones.
d. el
aumento de la dopamina no guarda relación con la actividad del núcleo acumben.
a y c
b y c
c y d
a y b
a y d
a y b
b y d
c y b
c y b
a y d
d y c
a y d
b y d
c y b
a y b
b y c
a y b
c y d
b y c
d y b
4. b y d
26.
La biosíntesis de la dopamina está relacionada con la de la noradrenalina y su degradación tiene
los mismos sistemas enzimáticos, sienembargo existe una diferencia entre ellas,
esta diferencia depende de
a.
las características del sistema enzimático.
b.
cual sea el primer sistema enzimático que actue.
c.
la reacción frente al sistema enzimático.
d.
no existe diferencia.
27.
La transmisión del impulso nervioso mediante la liberación de un
neurotransmisor es el mecanismo, que utiliza el sistema nervioso como medio de
comunicación, este mecanismo recibe el
nombre sinapsis y se caracteriza por,
a.
la comunicación previa del impulso nervioso. X
b.
el estado de los botones terminales. X
c.
la densidad del neurotransmisor.
c.
el ph de la membrana extracelular.
28.
El principio de Sir Henry Dale, fue fundamental para identificar el primer
neurotransmisor identificado en el sistema nervioso, este neurotransmisor es la
acetil colina, el principio considera,
a.
que las estructuras nerviosas son alterables por consiguiente su función.
b.
cuando una estructura colinérgica ó es
adrenérgica experimenta regeneración, su transmisor original es reestablecido.
c.
cuando una estructura colinérgica ó adrenérgica experimenta regeneración, su
transmisor es inalterable.
d. cuando una estructura colinérgica ó
adrenérgica experimenta regeneración el neurotransmisor además de
reestablecerse es inalterable.
1. a
y b
2.
b y d
3. a
y c
4. c
y d
29.
En la sinápsis existe una estructura que se llama receptor el cual es un
componente de la célula, éste receptor es capaz de identificar,
a.
una sustancia u hormona.
b.
una sustancia ó neurotransmisor.
c.
una sustancia ó péptido.
d.
una sustancia ó sales.
1.
a y b
2. b
y c
3. c
y d
4. a
y d
30.
La cascada de segundos mensajeros como consecuencia del aumento de la
concentración de Ca++ intracelular se mantiene un tiempo largo aún después de
que el estímulo ha cesado, genera en el tejido nervioso,
a.
sobresaturación por incrementos en la concentración del Ca++
b.
incapacidad de la célula para mantener un potencial de reposo.
c.
aceleración en la retroalimentación positiva, con la consecuente muerte celular.
d.
disminución del ph intracelular.
1. a
y d
2.
b y c
3. c
y d
4. a
y d